
金属の腐食とは、固体材料が環境によって純化学的反応または電気化学的反応によって変質破壊される現象をいいます。水溶液中や大気中で起る金属の腐食の大部分が電気化学的反応によります。
ここで、ひとことで腐食と言っても様々な種類の腐食があります。
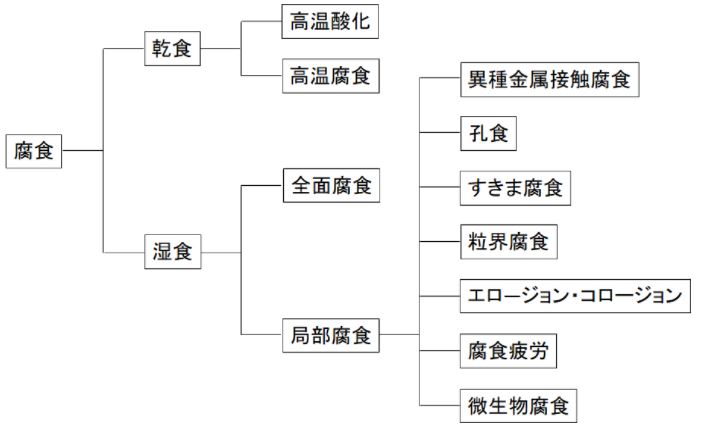
水分の存在する場合の腐食を湿食、高温の空気などの中で生じる腐食を乾食。
流体によって機械的に材料が侵される場合はエロージョン・コロージョン。
全面で起る均一腐食、部分的な局部腐食
結晶粒の間にそって進行する粒界腐食
被膜のピンホールなどから内部に向い進行する孔食、細いすきまで起るすきま腐食
応力のかかった部分で腐食とともに割れる応力腐食割れ
など様々な種類の腐食が存在します。
ここでは、さまざまな腐食について説明していきます。
Sponsored Link
錆(さび)
錆(さび)とは、一般的に腐食によって生成される腐食生成物が層になっている「赤錆」を指すことが多いですが、錆には赤錆以外にも下記のような種類の錆があります。
赤錆
鉄が酸化した状態。赤錆の被膜は外部の環境と遮断できないので、腐食が進み続きます。
黒錆
鉄が高温状況(水がない状況)で化学反応をしてできます。黒錆の被膜は外部の環境を遮断するので腐食が進行しづらくなります。
白錆
アルミニウムまたは亜鉛が酸化してできます。アルミニウムの白錆は大気中以外では腐食が進行します。亜鉛の白錆は腐食に強い性質を持っています。
青錆
銅が酸化した状態の錆です。青錆の被膜は外部の環境を遮断するので内部の腐食を防ぎます。
湿食と乾食
錆とは、腐食が進んだ際に作られる「腐食生成物」のことですが、この錆びの原因となる腐食にもいくつかの種類があります。そのもっとも大きな分類がこの湿食と乾食です。腐食の種類は数多くありますが、まずはこの湿食と乾食に分類することができます。その中でさらに細かい分類に分かれていくことになります。
湿食(しっしょく)
水が関わる腐食を言います。もっとも多岐にわたる腐食の大部分はこの湿食となり、一般的な腐食の進行は、水を媒介にしたイオンのやり取りによる電気化学反応として説明されます。通常の環境では、水に溶けた酸素や水素とともに腐食が進みます。酸素を消費する酸素消費型腐食と、水素イオンが酸化剤として作用する水素発生型腐食の二つが知られています。腐食の分類としては、湿食はさらに全面腐食と部分腐食に分けられます。
乾食(かんしょく)
腐食の発生に水が関わらないタイプの腐食を言います。酸素や周囲の雰囲気の元素と、金属が直接反応して腐食が進んでいく腐食で、高温環境で起きます。この際、周囲の酸素だけでなく、高温ガスと金属が反応することもあるため、酸素がない環境でも起きることがあります。乾食は、さらに高温酸化と高温腐食に分けられることがあります。高温酸化は、鉄の黒錆やスケールなどとして身近でも見られますが、高温腐食は、硫化腐食や窒化、浸炭酸化、高温ハロゲン腐食など腐食性のガスによって起きるものであり、化学プラントなど特殊な環境下で発生します。
全面腐食(均一腐食)
全面腐食(均一腐食)はもっとも基本的な腐食形態で、金属の表面全体が均一に腐食し、失われていく現象です。金属に含まれる不安定な原子が外へ飛び出すとき、安定状態の原子をプラス極、不安定な原子をマイナス極として、表面にごく微小なミクロ腐食電池を形成します。
腐食電池は金属の表面でランダムに発生し、どこか一カ所に偏るようなことはありません。そのため全面腐食が起こると、年月とともに少しずつ、かつ均一に金属表面が失われていきます。塩酸や硫酸、有機酸などといった酸化力の弱い環境で起こりやすく、屋外の大気中で起こる錆はほとんどがこの全面腐食です。
腐食の速度が遅く、損耗の程度も均一なため、対処はそれほど難しくありません。腐食速度から耐用年数を計算すれば、安全な板厚はすぐに求められます。また、環境に適した材質を選定することで、腐食そのものを防ぐことも可能です。
局部腐食(不均一腐食)
孔食
孔食は、金属の一部分のみで発生する局部腐食(不均一腐食)の一種です。キリで傷つけたような見た目で、進行すると金属の厚みを貫通してしまうこともあります。ステンレス鋼、アルミニウムといった、耐食性にすぐれた金属で起こりやすい腐食です。
さびにくいとされる金属のほとんどは、「不動態皮膜」という膜を表面にくまなく形成することで、腐食から守られています。しかしこの不動態皮膜は、一定の条件下で破壊され、機能を失ってしまうのです。
たとえばステンレス鋼の場合、海水中など、塩化物イオンが大量に存在する場所にあると、化学反応で不動態皮膜の維持に必要なクロムが不足し、不動態化ができなくなってしまいます。皮膜を失った部分から浸食され、部分的に深く腐食するのが孔食です。
孔食ができると、腐食部分(食孔)をマイナス極、腐食していない外部をプラス極としてマクロ腐食電池が形成されます。一度孔食が起きると、この腐食電池のはたらきによって内部の浸食が加速度的に進行し、腐食を食い止めることは困難です。孔食の発生を防ぐためには、酸化剤を添加して不動態皮膜を強化するか、孔食を促す塩素イオンや溶存酸素などの濃度を下げる必要があります。
すきま腐食
すきま腐食も、局部的に進む腐食の形態です。原理は孔食と同じで、ステンレス鋼をはじめとする不動態皮膜を形成しやすい金属が、皮膜の一部を失うことで起こります。異なるのは、金属の表面ではなく、金属板同士のすきまや、付着物とのすきまで腐食が発生するという点です。「すきま」という名前がついていますが、実際には10マイクロメートルにも満たないほどの、ごく小さな空間で起こっています。
腐食を防ぐ不動態皮膜の維持に必要なのが、溶存酸素です。しかしすきま内は非常に狭いため、酸素はすぐに底をついてしまいます。すると、酸素濃度が低いすきまの内側をマイナス極、濃度の高い外側をプラス極とする電池ができて電流が発生し、結果的にマクロ腐食電池が形成されます。電池形成後の腐食の進み方は、孔食と同じです。
海水中でステンレス鋼が腐食を起こす原因は、すきま腐食であることが多いと言われています。すきま腐食は、強い不動態皮膜を形成するクロムやチタンといった金属を使う、表面の付着物をこまめに取り除く、すきまができない構造を採用するといったことで防ぐことが可能です。
Sponsored Link
エロージョン・コロージョン
エロージョンとは、機械的に起こる磨耗作用のことで、コロージョンとは、腐食のことを言います。直訳すると、「磨耗的腐食」ということになります。
配管中を流れる水のように、腐食環境が流動していると、配管内面をこすることになり、流速が低ければ磨耗は起きませんが、流速が高ければ磨耗します。また、流体中に粉体など固体を含む場合には、激しく表面をこすり、機械的磨耗が生じます。
炭素鋼について考えると、炭素鋼は水や水溶液中で腐食しやすく、腐食すると、表面に錆びが発生します。この錆びが鋼材の表面を守り、錆びが全くない状態に比べると、腐食速度を大幅に低減できます。
しかし、このような状態のときに、流体による磨耗作用が働けば、その腐食生成物は削りとられることになり、新たな炭素鋼の表面が出現します。これに、水中に溶存している酸素が働けば腐食は当然促進されます。つまり、エロージョンによって錆びが取り除かれ、コロージョンによって錆びが発生じるという複合的な作用によって、いずれか一方の作用だけのときよりも、はるかに腐食速度は大きいものになります。
エロージョン・コロージョンが起き易いケースとしては、高速流の水や塩類の水溶液で、管内に乱流を生じることが多く、またそれ程高速流でなくても、曲がり部や熱交換器の入口などでも、乱流が発生するところがあります。このような場所ではエロージョン・コロージョンを起き易いとして知られております。
液体に固体が混じっていると、エロージョン・コロージョンを非常に発生し易く、石炭をパイプラインで輸送する配管などで、その例がみられます。
錆びに強いといわれているステンレス鋼は、エロージョン・コロージョンに強いといわれています。ステンレス鋼の不動態皮膜は、磨耗作用を受けても直ちに再生されるからです。しかし、海水ポンプのインペラーなどに使った場合、短時間でエロージョン・コロージョンを起す事例があるといわれています。
Sponsored Link
異種金属接触腐食
水中で異なる金属が接触しているときに、発生する腐食が異種金属接触腐食です。組み合わせた際にどちらかの金属がプラス極、一方がマイナス極となりますが、プラス極の金属のことを、より貴な金属や貴側の金属と呼びます。一方、マイナス極の金属のことをより卑な金属や卑側の金属と呼びます。なお、この順位を表したものが腐食電位列です。
多くの現場で使われている炭素鋼は、ステンレスやチタンなどの金属と接触するとマイナス極となるため腐食が促進されます。しかし、マグネシウムや亜鉛などと接触するとプラス極となるため、腐食は起こりにくくなります。
また、異種金属接触腐食の特徴は、卑な金属に対する貴な金属の面積比が腐食速度に影響を与える点にあります。たとえば、ステンレス鋼板に炭素鋼のボルトを用いて接合をするとボルトは急激に腐食しますが、その逆の場合、ボルトはあまり影響を受けません。
異種金属接触腐食を避けるためには異種金属を接触させないことが効果的ですが、実務では難しいと思います。この場合、面積比を考慮し腐食の影響を小さくしたり、塗装により防食したりする対策方法が現実的です。
もし、塗装をする場合は、腐食しやすい卑な金属だけに塗装することは避けましょう。これは、塗装では欠陥部が生じやすく、卑な金属でその部分で腐食が急速に進むためです。そのため、塗装を行うときには貴と卑のどちらにも行うとよいといわれています。
粒界腐食
金属は、多くの結晶粒子が集まり構成されています。結晶粒子の間のことを粒界と呼びますが、隣り合う結晶同士は原子の配列がずれているため不安定であり、腐食されやすくなります。通常の結晶であれば粒界で腐食することはありませんが、加熱により金属の組成は乱れ粒界腐食が起こります。
粒界腐食では、SUS304などのオーステナイト系ステンレス鋼を溶接する場合のものが有名です。ステンレス鋼は錆びにくい物質ですが、これは表面に不動態皮膜が生成されているためであり、この被膜にはクロムが欠かせません。ステンレスでは耐食性を発揮させるためにクロムを一定量以上配合させていますが、溶接などにより加熱したときにステンレス鋼に含まれている炭素とクロムが結合し、クロム炭化物を形成します。
炭化物は粒界で生成されますが、不動態皮膜の生成には役立ちません。そのため、ステンレス鋼の表面には不動態皮膜を持たない箇所が現れ、粒界に沿って腐食が進行していくのです。
粒界腐食を防止する対策は、炭素量の低いステンレス鋼を使用する、チタンやニオブなど炭素と結合しやすい元素を添加するなどがあります。
溶接部における選択腐食
金属と金属の溶接部は、腐食が起きやすい場所です。溶接部のみが選択的に腐食を受けることを、「溶接部の選択腐食」と呼んでいます。部分的に浸食が集中するため、短期間で板厚を貫通してしまうことも珍しくなく、溶接部の腐食は深刻な問題です。ここではステンレス鋼と炭素鋼の選択腐食について説明します。
ステンレス鋼は、500~900℃で加熱されると一定時間で鋭敏化する性質があります。鋭敏化とは、不動態皮膜の形成に必要なクロム含有量を、部分的に下回ることです。SUS304鋼の場合、700~800℃で熱された部分は数分という特に短い時間で鋭敏化します。鋭敏化した溶接部から、局所的に腐食が進むのです。また、溶接金属は組織が不均一になりやすく、クロムの含有量が偏ります。鋭敏化に加え、溶接金属のクロム濃度が低くなったところでも腐食が起こります。
炭素鋼の場合は、ステンレス鋼と違って鋭敏化による腐食は起こりません。工業用水や海水配管などでは、炭素鋼板を加熱せずに丸め、接続部だけを電気抵抗溶接で円筒状にする電縫溶接鋼管が使われています。加熱を受けた溶接部は、加熱されていない部分よりも腐食しやすい金属に変質しやすいため、溶接部に溝状の腐食が起こります。侵食の進行は非常に早く、1年で20A(2.3mm)や25A(3.2mm)の厚みを貫通してしまうことも珍しくありません。現在は、硫黄や銅の含有量を調整することで溶接部分の腐食を防ぐ、耐溝状腐食電縫鋼管が開発されています。
腐食割れの種類と対策
金属は、継続的に応力が加わったり、水素が急増されて脆弱性が増したりすることで、腐食割れを起こします。腐食割れは主に、応力腐食割れ・水素脆化割れ・腐食疲労の3つに分類でき、これらは発生の原因が異なり、対策方法も違うことに注意が必要です。それぞれの腐食割れについて仕組みの違いを見ていきましょう。
応力腐食割れ
応力腐食割れとは、金属に加わっている応力を原因として生じる腐食割れのことです。金属を引っ張って破断するに至る応力を引張強さと呼びますが、金属は、この引張強さ以下の小さな応力を加えても損傷を受けることはありません。
しかし、長時間継続的にこの応力が加わる環境下に置かれるとやがて割れが発生します。これが応力腐食割れの基本的なメカニズムです。応力腐食割れにつながる応力は、対象物の使用時にかかる応力や、加工時に蓄積された内部応力などの種類に分けられます。
応力腐食割れは、金属の素材と環境の組み合わせによって発生するので、特定の状況下においてのみ見られるものです。たとえば、炭素鋼が高温のNaNO3溶液に晒されることでNO3-が腐食割れを促すものや、黄銅がNH3を含む大気中に置かれることで、NH3が腐食割れを促すものが挙げられます。
また、高力アルミ合金や高力チタン合金が海水中に置かれることによって、CL-が原因となるケースも有名です。これらのような特定の素材と環境の組み合わせによって、素材が特定の状態に晒されることで、応力腐食割れが起こります。
水素脆化割れ
金属は腐食する時、水素イオンが電子を受け取ることで微量の原子状の水素(H)を表層に発生させるのが特徴です。ほとんどは表層への発生ですが、このうち一部が金属に吸蔵され、内部で拡散されていきます。引張応力を受けている金属は、金属内部の水素が格子欠陥などに集まり、脆化を起こしてしまい加わっている応力によって簡単に割れます。これが、水素脆化割れです。
応力の影響下にある金属の腐食割れという点では、応力腐食割れと共通しています。しかし、割れの発生原因が水素という点が大きく異なっています。また、水素脆化割れは、水素吸蔵が起こりやすい金属でのみ限定的に起こるものです。たとえば、高強度の鋼などが代表的な例で、応力腐食割れのしやすさとは別のベクトルから金属を考えなければなりません。
さらに、環境中に硫化水素、亜ヒ酸などが含まれていると水素脆化が起こりやすくなると言われています。これらの特定の物質が水素と結合して水素ガスとなるのを防ぐため、水素が原子状のまま留まり、金属内部に取り込まれやすくなるためです。
腐食疲労
金属は、引張強さ以下の応力であっても、繰り返し応力が加わることによって亀裂を生じ、破断されますが、これを一般的に金属疲労といい、専門的には単に疲労といいます。加わる応力が大きければ大きいほど、疲労は蓄積されやすく早い段階で破断に至るのはどの金属でもほぼ持ち合わせる性質です。
また、どんなに応力を加える回数を重ねても金属が損壊されない応力の限界があり、疲労限と呼びます。さらに、腐食による破断はさまざまな条件下で変化するのが金属疲労の特色でしょう。
たとえば、腐食環境下にある金属に疲労が生じた時、金属は通常の疲労時よりもさらに早い段階で破断を迎えます。それだけでなく、腐食環境においては金属の疲労限がなくなります。つまり、空気中など腐食の起こらない環境下においては疲労に至らなかったようなごく小さな応力であっても、腐食環境下になれば金属は破断される可能性あるということです。
関連図書